المحتويات
الدخيل الحيوي وأيض الأكسدة والاختزال
الديناميكا الحرارية للكائنات الحية
التنظيم والتحكم/التطور/الاستقصاء والمعالجة/التاريخ/انظر أيضًا
عملية الأيض💥 اي التمثيل الغذائي وتناول الاكسيجين وطاقة النمو ....
عملية الأيض💥
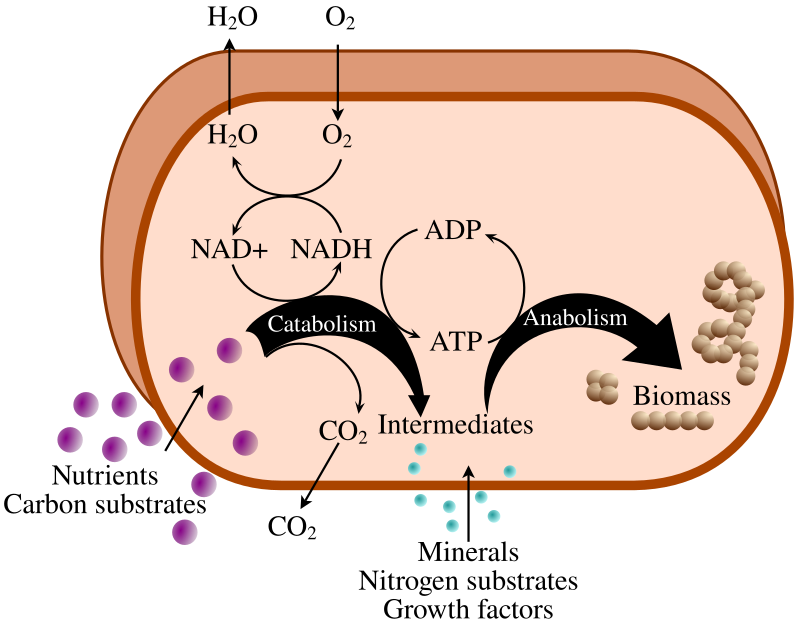
شرح مبسط للأيض في خلية
معلومات عامةصنف فرعي من
عملية حيوية
---------------------------------
كيمياء حيوية 💥
المكونات الرئيسية
جزيء حيوي
تمثيل غذائي
التاريخ والموضوعات
تاريخ
الكيمياء الحيوية
علم الخلية
المعلوماتية الحيوية
علم الإنزيمات
علم الوراثة
علم المناعة
علم الأحياء الجزيئي
كيمياء نباتية
علم الأحياء البنيوي
الأيض أو الاستقلاب (بالإنجليزية: Metabolism)
هو
مجموعة من التفاعلات الكيميائية في خلايا الكائن تحافظ على الحياة.
الأهداف الرئيسية الثلاث للأيض هي تحويل الغذاء/الوقود إلى طاقة لتشغيل
العمليات الخلوية، وتحويل الغذاء/الوقود إلى وحدات بناء للبروتينات،
والدهون، والأحماض النووية، وبعض السكريات، وإزالة الفضلات الأيضية
النيتروجينية. تلك التفاعلات التي تحفزها إنزيمات تسمح للكائنات بالنمو
والتكاثر، والمحافظة على تركيبها، والاستجابة للبيئة. يمكن أن يشير مصطلح
الأيض كذلك إلى مجموع كل التفاعلات الكيميائية التي تحدث في الكائنات
الحية، بما فيها الهضم ونقل المواد إلى وبين الخلايا المختلفة، وفي تلك
الحالة تسمى التفاعلات داخل الخلايا أيض وسيط أو أيض متوسط.
يُقسم
الأيض عادة إلى فئتين: التقويض، أي تكسير المواد العضوية، على سبيل المثال،
تكسير الجلوكوز إلى حمض البيروفيك بالتنفس الخلوي، وابتناء، أي بناء
مكونات الخلايا مثل البروتينات والأحماض النووية. عادة، يحرر التقويض طاقة
فيما يستهلك الابتناء الطاقة.
تُنظم تفاعلات الأيض الكيميائية في
مسارات أيضية، يحول من خلالها مركب كيميائي لآخر عبر سلسلة من الخطوات
بسلسلة من الإنزيمات. تعتبر الإنزيمات مصيرية بالنسبة للأيض لأنها تسمح
للكائنات بتنفيذ تفاعلات مرغوب بها تحتاج للطاقة ولن تحدث بنفسها دون
الإنزيمات، حيث تقوم الإنزيمات بدمجها بتفاعلات تلقائية تحرر طاقة. تعمل
الإنزيمات كمحفزات تسمح بحدوث التفاعلات بسرعة. تسمح الإنزيمات كذلك بتنظيم
المسارات الأيضية استجابةً للتغيرات في بيئة الخلية أو لإشارات من خلايا
أخرى.
يحدد النظام الأيضي لكائن معين أي المواد ستكون مغذية وأيها
تكون سامة. على سبيل المثال، بعض بدائيات النوى تستخدم كبريتيد الهيدروجين
كمغذي، إلا أن هذا الغار سام للحيوانات. تؤثر سرعة الأيض، ومعدل الأيض على
كم الغذاء الذي سيحتاجه الكائن، وكذلك على قدرته على الحصول على ذلك
الغذاء.
السمة اللافتة في عملية الأيض هي تشابه المسارات والمكونات
الأيضية الأساسية بين الأنواع المختلفة إلى حد كبير. على سبيل المثال،
مجموعة الأحماض الكربوكسيلية التي تشتهر بكونها مركبات وسيطة في دورة حمض
الستريك تتواجد في كل الكائنات المعروفة، حيث وجدت في كائنات متباينة
للغاية كبكتيريا إشريكية قولونية وحيدة الخلية والكائنات العملاقة متعددة
الخلايا مثل الأفيال.
التسميات العربيةتختلف ترجمة المصطلح العلمي
metabolism باختلاف الدول العربية حيث تستخدم تسمية أيض في مصر وفلسطين
والأردن والسعودية والعراق والإمارات واليمن وليبيا والجزائر والكويت. فيما
تستخدم تسمية استقلاب في سوريا. كما تستخدم تسمية تمثيل غذائي في مصر
أيضا.
المواد الكيميائية الحيوية الرئيسية
مزيد من المعلومات: جزيء حيوي، خلية والكيمياء الحيوية 💥
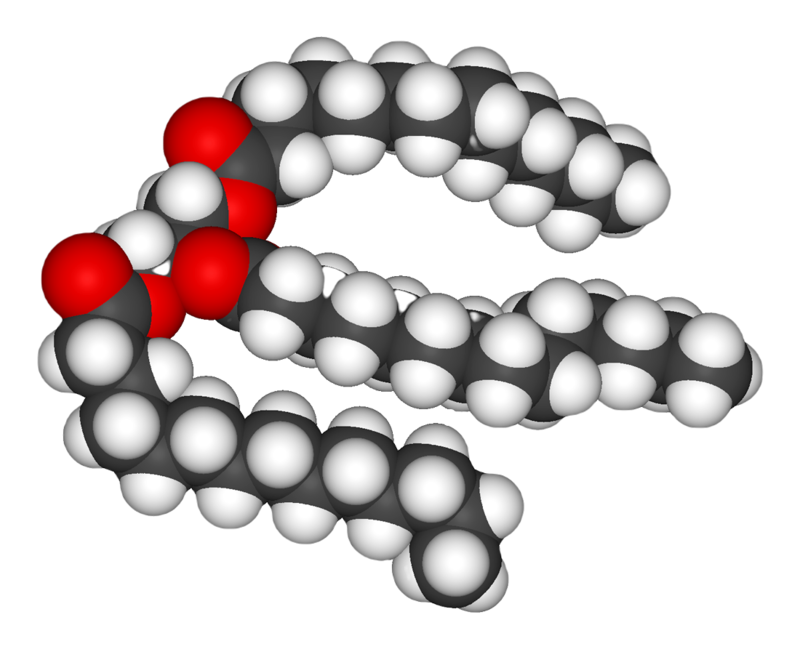 هيكل
ثلاثي الغليسريد ، عبارة عن جزيء غليسرين (أحمر) يرتبط به 3 أحماض دهنية
(رمادي وأسود)؛ ثلاثي الغلسريد هو جزيء دهني يمكن أن يختزن في الخلايا
الدهنية.
هيكل
ثلاثي الغليسريد ، عبارة عن جزيء غليسرين (أحمر) يرتبط به 3 أحماض دهنية
(رمادي وأسود)؛ ثلاثي الغلسريد هو جزيء دهني يمكن أن يختزن في الخلايا
الدهنية.
معظم الهياكل التي تشكل الحيوانات، النباتات والميكروبات
تتكون من ثلاث فئات أساسية من الجزيئات: حمض أميني، الكربوهيدرات والدهنيات
(وتسمى في كثير من الأحيان الدهون). وهي مصدر الطاقة المختزنة في الجسم
لاستخدامها وقت المجاعة أو أثناء الصوم. حيث أن هذه الجزيئات الحيوية
للحياة، التفاعلات الأيضية إما تركز على جعل هذه الجزيئات أثناء بناء
الخلايا والأنسجة، أو تقسيمها واستخدامها مصدر للطاقة وبالهضم. هذه المواد
الكيميائية الحيوية يمكن أن تدمج معا لصنع مبلمرات مثل الحمض النووي
الريبوزي المنقوص الأكسجين والبروتينات، الجزيئات الأساسية للحياة.
نوع الجزيء اسم الأشكال المونومرية اسم الأشكال المبلمرية أمثلة على الأشكال المبلمرية
حموض أمينية حموض أمينية بروتينات (تسمى أيضا عديدات الببتيد) بروتينات ليفية وبروتينات كروية
كربوهيدرات سكريات أحادية سكريات متعددة النشا، الغلايكوجين والسليلوز
حموض نووية نيوكليوتيدات عديدات النيوكليوتيد حمض نووي ريبوزي منقوص الأكسجين وحمض نووي ريبوزي
الأحماض الأمينية والبروتينات
تتكون
البروتينات من أحماض أمينية مرتبة في سلسلة طولية ترتبط معا بروابط
ببتيدية. العديد من البروتينات هي إنزيمات تحفز التفاعلات الكيميائية في
الأيض. تمتلك البروتينات الأخرى وظائف هيكلية أو ميكانيكية، مثل البروتينات
التي تشكل الهيكل الخلوي، وهو نظام من السقالة يحافظ على شكل الخلية. كذلك
فإن البروتينات مهمة في تأشير الخلية، واستجابة المناعة، والتصاق الخلايا،
والنقل النشط عبر الأغشية، ودورة الخلية. تساهم الأحماض الأمينية أيضا في
أيض الطاقة الخلوي بتوفير مصدر للكربون للدخول في دورة حمض الستريك، بالأخص
حين يكون مصدر الطاقة الرئيسي، مثل الجلوكوز، نادرًا، أو حين تكون الخلايا
تحت إجهاد أيضي.
الدهون
الدهون هي المجموعة الأكثر تنوعًا
من المواد الكيماوية الحيوية. استخداماتها الهيكلية الرئيسية هي كونها جزء
من الأغشية الحيوية سواء الداخلية أو الخارجية، مثل غشاء الخلية، أو كمصدر
للطاقة. تُعرف الدهون عادة على أنها جزيئات حيوية كارهة للماء أو مزدوجة
الألفة ولكن تذوب في المذيبات العضوية مثل البنزين أو كلوروفورم. الدهون هي
مجموعة كبيرة من المركبات التي تحتوي على أحماض دهنية وغليسرول، جزئ
غليسرول مرتبط بـ3 إسترات أحماض دهنية يسمى ثلاثي الغليسريد. تتواجد العديد
من التنوعات على الهيكل الأساسي، بما في ذلك هياكل بديلة مثل سفينغوزين في
الشحميات السفينجولية، ومجموعات محبة للماء مثل الفوسفات في الدهن
الفسفوري. ستيرويدات مثل الكولسترول هي فئة أخرى كبيرة من الدهون.
السكريات 💥
الجلوكوز يمكن أن يتواجد في شكل سلسلة مستقيمة أو حلقة.
الكربوهيدرات
هي ألدهيدات أو كيتونات، مع العديد من مجموعات الهيدروكسيل المرتبطة بها.
يمكنها التواجد في صورة سلاسل مستقيمة أو حلقات. السكريات هي الجزيئات
الحيوية الأكثر وفرة، وتؤدي العديد من الأدوار، مثل تخزين ونقل الطاقة
(نشا، وغلايكوجين)، وكونها مكونات هيكلية (سليولوز في النبات، وكايتين في
الحيوانات). تسمى وحدات السكريات الأساسية سكر أحادي وتشمل جالاكتوز،
وفركتوز، والأهم الجلوكوز. يمكن أن ترتبط السكريات الأحادية معا لتكوين
متعدد السكاريد.
النوكليوتيداتالحمضان النوويان، حمض نووي ريبوزي
منقوص الأكسجين (DNA) وحمض نووي ريبوزي (RNA) هما بوليمران للنوكليوتيدات.
يتكون كل نوكليوتيد من مجموعة فوسفات ترتبط بسكر الريبوز أو ريبوز منقوص
الأكسجين والذي يرتبط بقاعدة نيتروجينية. تعد الأحماض النووية هامة لتخزين
واستعمال المعلومات الوراثية، وترجمتها عبر عمليات النسخ، والاصطناع الحيوي
للبروتين. تُحمى هذه المعلومات بآليات ترميم الدنا وتنتشر بتضاعف الحمض
النووي الريبوزي منقوص الأكسجين. تمتلك العديد من الفيروسات جينوم من الحمض
النووي الريبوزي، مثل فيروس العوز المناعي البشري، الذي يستخدم الانتساخ
العكسي لصنع نموذج DNA من جينوم الـRNA. الـRNA في إنزيمات الحمض النووي
الريبوزي مثل جسيمات التضفير والريبوسومات تشبه الإنزيمات في قدرتها على
تحفيز التفاعلات الكيميائية. تُكون النيوكليوسيدات بارتباط قاعدة نووية
بسكر ريبوز. تلك القواعد هي عبارة عن مركبات حلقية غير متجانسة تحتوي على
النيتروجين، وتصنف إما بيورينات أو بيريميدينات. تعمل النوكليوتيدات كعوامل
مرافقة في تفاعلات الأيض.
العوامل المرافقة 💥
تركيب أسيتيل مرافق الإنزيم-أ مجموعة الأسيتيل المتنقلة ترتبط بذرة الكبريت في أقصى اليسار.
يتضمن
الأيض مجموعة شاسعة من التفاعلات الكيميائية، لكن أغلبها يقع تحت أنواع
أساسية قليلة من التفاعلات التي تتضمن انتقال مجموعات وظيفية من الذرات
وروابطها بين الجزيئات. تسمح الكيمياء المشتركة للخلايا باستخدام مجموعة
صغيرة من الوسائط الأيضية لحمل المجموعات الكيميائية بين التفاعلات
المختلفة. تلك الوسائط الناقلة للمجموعات تسمى عوامل مرافقة. تُنفذ كل فئة
من التفاعلات الناقلة للمجموعات بعامل مرافق معين، وهو ركيزة لمجموعة من
الإنزيمات التي تنتجه، ومجموعة من الإنزيمات التي تستهلكه. لذلك düvd تصنيع
واستهلاك وإعادة تدوير تلك العوامل المرافقة باستمرار.
عامل مرافق
مركزي هو أدينوسين ثلاثي الفوسفات (ATP)، العملة الموحدة للطاقة في
الخلايا. يستخدم هذا النوكليوتيد لتقل الطاقة الكيميائية بين التفاعلات
الكيميائية المختلفة. توجد كمية قليلة من ATP في الخلايا، ولكن يُولد عادة
باستمرار، يمكن أن يستخدم الجسم البشري وزنه من الـATP في اليوم. يعمل
أدينوسين ثلاثي الفوسفات كجسر بين التقويض والابتناء. يقوم التقويض بتكسير
الجزيئات، ويضعهم الابتناء معًا. تولد تفاعلات التقويض ATP، فيما تستهلكه
تفاعلات الابتناء. كما يعمل أيضا كحامل لمجموعات الفوسفات في تفاعلات
الفسفرة.
الفيتامين هو مركب عضوي يحتاجه الجسم بكميات صغيرة ولا
يمكن تصنيعه في الخلايا. في تغذية الإنسان، تعمل أغلب الفيتامنيات كعوامل
مرافقة بعد التعديل، على سبيل المثال، كل الفيتامينات التي تذوب في الماء
تنم فسفرتها أو ترتبط بالنوكليوتيدات حين تُستخدم في الخلايا.ثنائي
نوكليوتيد الأدنين وأميد النيكوتين (NAD+)، أحد مشتقات فيتامين ب3
(نياسين)، يعد عامل مرافق مهم يعمل كمستقبل للهيدروجين. تقوم مئات الأنواع
المنفصلة من الإنزيمات نازعة الهيدروجين بنزع الإلكترونات من ركائزها
وتختزل NAD+ إلى NADH. تلك الصورة المختزلة من العامل المرافق تصبح ركيزة
للعديد من الإنزيمات المختزلة في الخلية.
يتواجد ثنائي نوكليوتيد
الأدنين وأميد النيكوتين في شكلين مرتبطين في الخلية، NADH وNADPH. الشكل
الأول NAD+/NADH هو أكثر أهمية في تفاعلات التقويض، بينما يستخدم
NADP+/NADPH في تفاعلات الابتناء.
تركيب الهيموغلوبين. وحدات البروتين بالأحمر والأزرق، والمجموعات التي تحتوي على الهيم بالأخضر. من ببب: 1GZX.
المعادن
والعوامل المرافقةتلعب العناصر غير العضوية أدوارًا هامة في الأيض، بعضها
وفير (مثل الصوديوم، والبوتاسيوم) فيما يؤدي البعض الآخر وظائفه في تركيزات
دقيقة. تتكون نحو 99% من كتلة الثدييات من العناصر التالية: كربون،
ونيتروجين، وكالسيوم، وكلور، وبوتاسيوم، وهيدروجين، وفوسفور، وأكسجين،
وكبريت.
تحتوي المركبات العضوية (البروتينات، والدهون، والسكريات)
على أغلب الكربون والنيتروجين، يتواجد أغلب الأكسجين والهيدروجين في صورة
ماء.
تعمل العناصر غير العضوية الوفيرة ككهارل أيونية. الأيونات
الأكثر أهمية هي الصوديوم، والبوتاسيوم، والكالسيوم، والماغنسيوم، والكلور،
والفوسفات، والأيون العضوي بيكربونات. المحافظة على تدرج أيوني دقيق عبر
الأغشية الخلوية يحافظ على الضغط الإسموزي والأس الهيدروجيني. الأيونات
مهمة كذلك لوظيفة الأعصاب والعضلات، حيث يُنتج جهد الفعل في تلك الأنسجة
بتبادل الكهارل بين السائل خارج خلوي وسائل الخلية (عصارة خلوية). تدخل
الكهارل الخلايا وتغادرها عبر بروتينات في غشاء الخلية تسمى قنوات أيونية.
على سبيل المثال، يعتمد الانقباض العضلي على حركة الكالسيوم، والصوديوم،
والبوتاسيوم عبر القنوات الأيونية في غشاء الخلية والأنيبيبات
المستعرضة.توجد الفلزات الانتقالية عادة في صورة عناصر شحيحة في الكائنات،
ويعد الحديد والزنك الأكثر وفرة. تستخدم تلك الفلزات في بعض البروتينات
كعوامل مرافقة وهي ضرورية لنشاط إنزيمات مثل كاتالاز والبروتينات الحاملة
للأكسجين مثل الهيموغلوبين.
التفاعلات
تنقسم تفاعلات الاستقلاب إلى:
1-
تفاعلات الهدم Catabolism: حيث تُكسر المواد الغذائية الرئيسية سواء كانت
كربوهيدرات أو بروتينات أو دهون خلال طرق مختلفة من التفاعلات الحيوية إلى
جزيئات بسيطة وينتج عن ذلك الحصول على الطاقة.
2-تفاعلات البناء
(Anabolism): الجزيئات البسيطة الناتجة من عملية الهدم يمكن استخدامها
كنواة لبناء مواد أكثر تعقيداً سواء كانت بروتينية أو أحماض نووية من خلال
سلسلة من التفاعلات وذلك لبناء الأنسجة وتستهلك طاقة في تلك التفاعلات.
تأخذ
عمليات البناء والهدم مسارات مختلفة من ناحية التفاعلات الحيوية داخل جسم
الكائن الحي، تُحوّل فيها المواد الكيميائية بسلسلة من الأنزيمات.هذه
الأنزيمات هي حاسمة لعملية التمثيل الغذائي حيث تعمل على تسريع التفاعلات
وتكون مهمة جداً في الحفاظ على حياة الخلية.
أحد السمات البارزة في عملية الأيض هو التشابه في المسارات الأساسية بين كائنات تختلف اختلافاً شاسعاً عن بعضها البعض.
معظم
الهياكل التي تشكل الحيوانات والنباتات والميكروبات مصنوعة من ثلاث فئات
أساسية من الجزيئات: الأحماض الأمينية، الكربوهيدرات، والدهون. ووظيفة
التمثيل الغذائي تتركز في استخدام هذه الجزيئات في بناء الخلايا والأنسجة،
أو تقسيمها واستخدامها كمصدر للطاقة. ويمكن أن تجتمع هذه المواد الكيميائية
لتشكل بوليمرات مثل الحمض النووي والبروتينات.
ويبدأ استقلاب
الكربوهيدرات مع امتصاص الغلوكوز عبر جدران الأمعاء إلى الدم فيحمل البعض
منه إلى مختلف أنحاء الجسم حيث يُستقلب في حين يُخزّن البعض الآخر في الكبد
والعضلات على شكل سكر أو غلايكوجين وتتفكك بعد ذلك عند الحاجة.
التقويضالتقويض
هو مجموعة من العمليات الأيضية التي تقوم بتكسير الجزيئات الكبيرة. تشمل
تلك التفاعلات تكسير وأكسدة جزيئات الطعام. الهدف من تفاعلات التقويض هو
توفير الطاقة والمكونات المطلوبة في تفاعلات الابتناء التي تبني الجزيئات.
تختلف طبيعة تلك التفاعلات من كائن لآخر، ويمكن تقسيم الكائنات وفقًا
لمصادر الطاقة والكربون الخاصة بهم (مجموعات غذائية أساسية)، كما يتضح في
الجدول بالأسفل. تستخدم الكائناتُ عضوية التغذية الجزيئاتِ العضوية مصدرًا
للطاقة، فيما تستخدم الكائنات جمادية التغذية ركائز غير عضوية، وتستخدم
الكائنات ضوئية التغذية ضوء الشمس كطاقة كيميائية. على أي حال، تعتمد كل
تلك الأشكال المختلفة من الأيض على تفاعلات أكسدة-اختزال تتضمن انتقال
إلكترونات من متبرع مختزَل مثل المركبات العضوية، أو الماء، أو الأمونياك،
أو كبريتيد الهيدروجين، أو حديدوز إلى جزيئات مستقبلة مثل الأكسجين، أو
النترات، أو الكبريتات. في الحيوانات، تتضمن تلك التفاعلات مركبات عضوية
معقدة تُكسّر إلى جزيئات أبسط، مثل ثنائي أكسيد الكربون والماء. في كائنات
البناء الضوئي، مثل النباتات والبكتيريا الزرقاء، لا تُطلق تلك التفاعلات
الناقلة للإلكترونات طاقة وإنما تستعمل كطريقة لتخزين الطاقة الممتصة من
ضوء الشمس.
تصنيف الكائنات وفقا لأيضهم 💥 مصدر الطاقة ضوء الشمس ضوئية- -التغذية
الجزيئات المشكلة سابقا كيميائية-
المتبرع بالإلكترون مركبات عضوية عضوية-
مركبات لاعضوية جمادية-
مصدر الكربون مركبات عضوية غيري-
مركبات لاعضوية ذاتية-
يمكن
فصل المجموعة الأكثر شيوعًا من تفاعلات التقويض في الحيوانات إلى 3 مراحل
رئيسية. في المرحلة الأولى، تُهضم مركبات عضوية كبيرة، مثل البروتينات، أو
متعددات السكاريد، أو الدهون إلى مكوناتهم الأصغر خارج الخلايا. المرحلة
التالية، تستوعب الخلايا تلكَ الجزيئاتِ الأصغرَ وتحولها لجزيئات أصغر،
عادة أسيتيل مرافق الإنزيم-أ، الذي يطلق بعض الطاقة. أخيرا، مجموعة
الأسيتيل الموجودة في أسيتيل مرافق الإنزيم-أ تُؤكسد إلى ماء وثنائي أكسيد
الكربون في دورة حمض الستريك وسلسلة نقل الإلكترون، ما يحرر طاقة تُخزن
باختزال العامل المرافق ثنائي نوكليوتيد الأدنين وأميد النيكوتين (NAD+)
إلى NADH.
الهضم
الجزيئات الضخمة مثل النشا، أو السليولوز،
أو البروتينات لا تستوعبها الخلايا بسرعة ويجب تكسيرها لوحدات أصغر قبل
استخدامها في أيض الخلية. العديد من فئنات الإنزيمات المشتركة تهضم تلك
البوليمرات. تلك الإنزيمات الهضمية تشمل ببتيداز الذي يهضم البروتينات إلى
أحماض أمينية، بالإضافة إلى هيدروليزات الغلايكوسيد التي تهضم متعددات
السكاريد إلى سكريات بسيطة تعرف باسم سكر أحادي.
تفرز الميكروبات
ببساطة إنزيمات هضمية إلى البيئة المحيطة بها، بينما تستطيع الحيوانات
إفراز تلك الإنزيمات فقط من خلايا متخصصة في قناتها الهضمية التي تشمل
الغدد اللعابية، والمعدة، والبنكرياس. الأحماض الأمينية، أو السكريات
الناتجة عن تلك الإنزيمات تضخها بروتينات النقل النشط إلى لاخل الخلايا.
الطاقة من المركبات العضوية 💥
مخطط مبسط للمرحلة الأولى لفك البروتينات، والسكريات، والدهون (ينتج Acetyl-CoA).
تقويض
السكريات هو تكسير السكريات إلى وحدات أصغر. عادة ما تُستوعب السكريات
لداخل الخلايا بمجرد أن تُهضم إلى سكريات أحادية. بمجرد دخولها، الطريقة
الأكبر للتحلل هي تحلل الجلوكوز، والتي يحول فيها السكريات مثل الجلوكوز
والفركتوز إلى حمض البيروفيك مع توليد بعض جزيئات أدينوسين ثلاثي الفوسفات
(ATP).
حمض البيروفيك هو مركب وسيط في العديد من المسارات الأيضية،
لكن أغلبه يُحول إلى أسيتيل مرافق الإنزيم-أ بتحلل الجلوكوز الهوائي ويُقدم
لدورة حمض السيتريك. رغم أنه يُلد المزيد من ATP في دورة حمض الستريك، فإن
المنتج الأهم هو NADH الذي يُصنع من NAD+ عند أكسدة أسيتيل مرافق
الإنزيم-أ. تحرر الأكسدة ثنائي أكسيد الكربون كمخلف للتفاعل. في الظروف
اللاهوائية، يُنتج تحلل الجلوكوز حمض اللبنيك، بقيام إنزيم نازع لهيدروجين
اللاكتات بإعادة أكسدة NADH إلى NAD+ ليُستخدم مجددا في تحلل الجلوكوز.
طريق بديل لتكسير الجلوكوز هو مسار فوسفات البنتوز، الذي يختزل العامل
المرافق فوسفات ثنائي نيوكليوتيد الأدينين وأميد النيكوتين NADPH وينتج
سكريات خماسية مثل الريبوز.
تُقوّض الدهون بالتحلل المائي إلى أحماض
دهنية حرة وغليسرول. يدخل الغليسرول في مسار تحلل الجلوكوز بينما تُكسر
الأحماض الدهنية بأكسدة الحمض الدهني لتحرير أسيتيل مرافق الإنزيم-أ، الذي
يُقدم لدورة حمض الستريك. تطلق الأحماض الدهنية طاقة أكبر من السكريات عند
أكسدتها لأن السكريات تحتوي على أكسجين أكثر في تركيبها. تُحلل الستيرويدات
أيضا في بعض البكتيريا في عملية مشابهة لأكسدة الحمض الدهني، وتشمل عملية
التحلل تلك إطلاق كميات كبيرة من أسيتيل مرافق الإنزيم-أ، وبروبيونيل مرافق
الإنزيم-أ، وحمض البيروفيك، والذين يمكن استخدامهم جميعا بالخلية مصدرًا
للطاقة. بكتيريا المتفطرة السلية يمكنها أن تنمو اعتمادا على الكولسترول
مصدرًا وحيدًا للكربون، وجرى التحقق من صحة أن الجينات المشاركة في مسارات
استهلاك الكولسترول مهمة خلال مراحل متنوعة من دورة حياة العدوى لبكتيريا
المتفطرة السلية.تُستخدم الأحماض الأمينية إما لتصنيع البروتينات والجزيئات
الحيوية الأخرى، وإما مصدرًا للطاقة بأكسدتها إلى يوريا وثنائي أكسيد
الكربون. يبدأ مسار الأكسدة بنزع مجموعة الأمين بناقلة الأمين. تُقدّم
مجموعة الأمين لدورة اليوريا، ما يترك هيكل كربوني منزوع الكربون في صورة
حمض كيتو. العديد من أحماض الكيتو تلك تعد مركبات وسيطة في دورة حمض
الستريك، على سبيل المثال نزع الأمين من حمض الجلوتاميك يكوِّن حمض ألفا
كيتوجلوتاريك. يمكن كذلك تحويل الأحماض الأمينية المنتجة للجلوكوز إلى
جلوكوز، من خلال استحداث الجلوكوز.
تحويل الطاقة
فسفرة تأكسدية
في
الفسفرة التأكسدية، تُزال الإلكترونات من الجزيئات العضوية في مناطق مثل
دورة حمض البروتاغون وتحول لأكسجين وتستخدم الطاقة المتحررة في تصنيع
أدينوسين ثلاثي الفوسفات (ATP). يجري ذلك في حقيقيات النوى بسلسلة من
البروتينات في أغشية الميتوكوندريا تعرف باسم سلسلة نقل الإلكترون. في
بدائيات النوى، توجد تلك البروتينات في الغشاء الداخلي للخلية. تستخدم تلك
البروتينات الطاقة المتحررة من الالكترونات المارة عبر الجزيئات المختزلة
مثل NADH لضخ البروتونات عبر الغشاء.
💥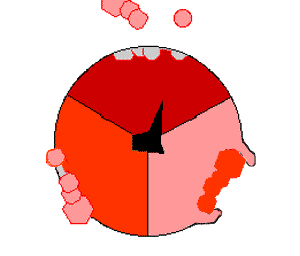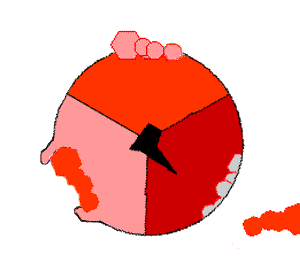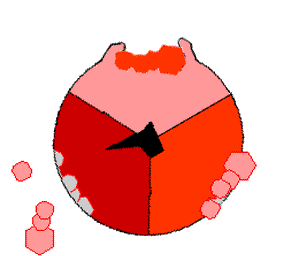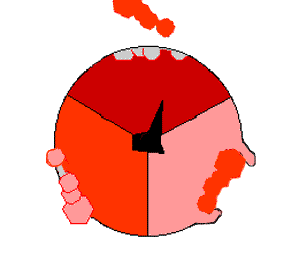
آلية أيه تي بي سينثاز. يظهر ATP باللون الأحمر، و ADP ،و الفوسفات باللون الوردي والوحدة الدوارة الدورية باللون الأسود.
ضخ البروتونات خارج الميتوكندريا يخلق فرق في تركيز البروتون عبر الغشاء ويولد تدرج كهروكيميائي.
تقود
هذه القوة البروتونات مرة أخرى لداخل الميتوكندريا بقاعدة إنزيم يسمى أيه
تي بي سينثاز. يجعل تدفق البروتونات الوحدة الدوارة تدور، ما يغير من شكل
الموقع النشط في الإنزيم ويقوم بفسفرة ADP محولا إياه إلى ATP.
طاقة
من المركبات غير العضويةجمادي التغذية الكيميائي هو نوع من الأيض يوجد في
بدائيات النوى حيث يُحصل على الطاقة من أكسدة المركبات غير العضوية. يمكن
لتلك المتعضيات استخدام الهيدروجين، أو مركبات الكبريت المختزلة (مثل
الكبريتيد، وكبريتيد الهيدروجين، وثيوكبريتات)، أوأكسيد الحديد الثنائي، أو
الأمونيا كمصادر لاختزال الطاقة ويحصلون على الطاقة بأكسدة تلك المركبات
بواسطة قابلات الإلكترونات مثل الأكسجين أو النتريت. تلك العمليات
الميكروبية مهمة في الدورات الحيوية الجيولوجية الكيميائية العامة مثل
تكوين الأسيتون، والنترجة، ونزع النيتروجين وهي عمليات مهمة لخصوبة التربة.
طاقة
من الضوءتنتزع النباتات، والبكتيريا الزرقاء، والبكتيريا الأرجوانية،
والخضربيات وبعض الطلائعيات الطاقة من ضوء الشمس. ترتبط هذه العملية عادة
بتحويل ثنائي أكسيد الكربون إلى مركبات عضوية، كجزء من البناء الضوئي. يمكن
مع ذلك أن تجري العمليتان بشكل منفصل كما في بدائيات النوى، كما يمكن
للبكتيريا الأرجوانية، والخضربيات استخدام ضوء الشمس كمصدر للطاقة مع
التنقل بين تثبيت الكربون أو تخمير المواد العضوية.في العديد من المتعضيات
يشبه انتزاع الطاقة الشمسية في المبدأ الفسفرة التأكسدية، حيث يشمل تخزين
الطاقة في صورة فرق تركيز لبروتون. ذلك الفرق في التركيز هو الذي يؤدي
لتصنع ATP. تأتي الإلكترونات المطلوبة لسلسة نقل الإلكترون من بروتينات
جامعة للضوء تسمى رودوبسين أو مراكز رد فعل البناء الضوئي. تُقسم مراكز رد
الفعل إلى نوعين على حسب نوع صبغة البناء الضوئي الموجودة، تملك أغلب
البكتيريا البانية للضوء نوع واحد، فيما تملك النباتات والبكتيريا الزرقاء
نوعين.في النباتات، والطحالب، والبكتيريا الزرقاء، تستخدم وحدات النظام
الثاني للبناء الضوئي الطاقة الضوئية لإزالة الإلكترونات من الماء، وتحرير
الأكسجين كمخلف للتفاعل. تتدفق الإلكترونات بعد ذلك إلى سيتوكروم b6f
complex، الذي يستخدم طاقتهم لضخ البروتونات عبر غشاء الثايلاكويد في
البلاستيدات الخضراء. تنتقل تلك البروتونات مرة أخرى عبر الغشاء حيث تدفع
أيه تي بي سينثاز -كما سبق-. تتدفق الإلكترونات بعد ذلك عبر وحدات النظام
الأول للبناء الضوئي ويمكنها بعد ذلك إما أن تختزل تميم الإنزيم NADP+،
لاستخدامه في دورة كالفين، أو أن يعاد تدويرها لتوليد المزيد من ATP.
الابتناء
الابتناء
هو مجموعة من العمليات الأيضية البناءة تُستخدم فيها الطاقة المتحررة من
التقويض لتصنيع جزيئات معقدة. عمومًا، تُصنع الجزئيات المعقدة التي تكون
التركيب الخلوي خطوة بخطوة من مركبات طليعية صغيرة وبسيطة. يشمل الابتناء 3
مراحل أساسية. أولا، إنتاج المركبات الطيلعية مثل الأحماض الأمينية،
والسكر الأحادي، وتربينويد، ونوكليوتيدات، وثانيا، تنشيطهم إلى صور متفاعلة
باستخدام الطاقة من أدينوسين ثلاثي الفوسفات، وثالثا، تجميع تلك المركبات
الطليعية لتكوين جزيئات معقدة مثل البروتينات، ومتعددات السكاريد، والدهون،
والأحماض النووية.
تختلف الكائنات من حيث عدد الجزيئات التي تُبنى
في خلاياها. الكائنات ذاتية التغذية مثل النباتات يمكنها بناء الجزيئات
العضوية المعقدة في الخلايا مثل متعددات السكاريد والبروتينات من جزيئات
بسيطة مثل ثنائي أكسيد الكربون والماء. الكائنات غيرية التغذية في المقابل،
تحتاج لمصدر للمواد الأكثر تعقيدا، مثل السكريات الأحادية والأحماض
الأمينية، لإنتاج تلك الجزيئات المعقدة. يمكن تصنيف الكائنات بحسب المصدر
النهائي للطاقة: تحصل الكائنات ضوئية التغذية، والكائنات الضوئية غيرية
التغذية على الطاقة من الضوء، بينما تحصل الكائنات كيميائية التغذية،
والكائنات كيميائية غيرية التغذية على الطاقة من تفاعلات أكسدة غير عضوية
تثبيت الكربون  خلايا نبانية (محاطة بجدران بنفسجية) مليئة بالبلاستيدات الخضراء، وهي موقع البناء الضوئي
خلايا نبانية (محاطة بجدران بنفسجية) مليئة بالبلاستيدات الخضراء، وهي موقع البناء الضوئي
البناء
الضوئي هو تصنيع الكربوهيدرات من ضوء الشمس وثنائي أكسيد الكربون في
النبات، والبكتيريا الزرقاء، والطحالب، البناء الضوئي الأكسجيني يقسم
الماء، وينتج الأكسجين كمخلفات للتفاعل. تستخدم هذه العملية أدينوسين ثلاثي
الفوسفات (ATP) وثنائي نوكليوتيد الأدنين وأميد النيكوتين (NADPH)
الناتجان عن مراكز رد فعل البناء الضوئي لتحويل ثنائي أكسيد الكربون إلى
حمض 3-فوسفوغليسيريك، الذي يمكن تحويله بعد ذلك إلى جلوكوز. يُنفّذ تفاعلَ
تثبيت الكربون إنزيمُ روبيسكو كجزء من دورة كالفين. يحدث 3 أنواع من البناء
الضوئي في النباتات: تمثيل ضوئي ثلاثي الكربون، وتمثيل ضوئي رباعي
الكربون، وأيض حامض المخلدات. الفرق بين أولئك هو الطريق الذي يسلكه ثنائي
أكسيد الكربون نحو دورة كالفين، ففي ثلاثي الكربون يقوم النبات بتثبيت
ثنائي أكسيد الكربون مباشرة، أما في النوعين الآخرين يدمج البناء الضوئي
ثنائي أكسيد الكربون في المركبات الأخرى أولا، كطريقة للتكيف مع ضوء الشمس
القوي والظروف الجافة.في بدائيات النوى التي تقوم بالبناء الضوئي، آليات
تثبيت الكربون أكثر تنوعا. حيث يمكن تثبيت ثنائي أكسيد الكربون بدورة
كالفين، وهي دورة حمض الستريك ولكن معكوسة، أو بإضافة كربوكسيل لأسيتيل
مرافق الإنزيم-أ. بدائيات النوى كيميائية التغذية تثبت ثنائي أكسيد الكربون
عبر دورة كالفين، ولكنها تستخدم الطاقة الصادرة من المركبات غير العضوية
لتحفيز التفاعل.
السكريات والغليكاناتفي ابتناء السكريات، يمكن تحويل
الأحماض العضوية البسيطة إلى سكريات أحادية مثل الجلوكوز ثم تجميعها لتكوين
متعددات السكاريد مثل النشا. توليد الجلوكوز من مركبات مثل حمض البيروفيك،
وحمض اللبنيك، وغليسرول، وحمض 3-فوسفوغليسيريك، والأحماض الأمينية يسمى
استحداث الجلوكوز. يحول استحداث الجلوكوز حمض البيروفيك إلى جلوكوز
6-فوسفات عبر سلسلة من المركبات الوسطية، تشترك العديد منها في تحلل
الجلوكوز. على أي حال، هذا المسار ليس مجرد تحلل الجلوكوز بشكل معكوس، حيث
أن العديد من الخطوات تُحفزها إنزيماتٌ غير موجودة في تحلل الجلوكوز. هذا
الأمر مهم حيث يسمح بتنظيم تكوين وتكسير الجلوكوز بشكل منفصل، ويمنع حدوث
المسارين بالتزامن في حلقة مفرغة.رغم أن الدهون هي طريقة شائعة لتخزين
الطاقة، في الفقاريات مثل الإنسان لا يمكن تحويل الأحماض الدهنية في تلك
المخازن إلى جلوكوز من خلال استحداث الجلوكوز حيث أن تلك الكائنات لا
يمكنها تحويل أسيتيل مرافق الإنزيم-أ إلى حمض البيروفيك، تمتلك النباتات
الإنزيمات الضرورية لذلك بينما لا تمتلكها الحيوانات. نتيجة لذلك، بعد فترة
طويلة من المجاعة، تحتاج الفقاريات لإنتاج أجسام كيتونية من الأحماض
الدهنية لاستبدال الجلوكوز في الأنسجة مثل المخ الذي لا يستطيع أيض الأحماض
الدهنية. في الكائنات الأخرى كالنباتات والبكتيريا، تُحل تلك المشكلة
الأيضية بدورة الجلايكسولات، التي تتجاوز خطوة نزع الكربوكسيل الموجودة في
دورة حمض الستريك وتسمح بتحول أسيتيل مرافق الإنزيم-أ إلى حمض
أكسالوأسيتيك، الذي يمكن استخدامه لإنتاج الجلوكوز.تُصنع متعددات السكاريد
والغليكانات بإضافة متتابعة للسكريات الأحادية بإنزيم ناقل الغليكوزيل من
سكر-فوسفات تفاعلي متبرع مثل غلوكوز ثنائي فوسفات اليوريدين إلى مجموعة
هيدروكسيل مستقبلة على متعدد السكاريد النامي. نظرًا لأن أي من مجموعات
الهيدروكسيل على حلقة المادة المتفاعلة يمكن أن تكون مستقبلة، يمكن أن يكون
متعدد السكاريد الناتج إما متفرع أو مستقيم. يمكن أن تمتلك متعددات
السكاريد الناتجة وظائف تركيبية أو أيضية، أو تُحول إلى دهون أو بروتينات.
الأحماض الدهنية، وتربينويد، وستيرويدات 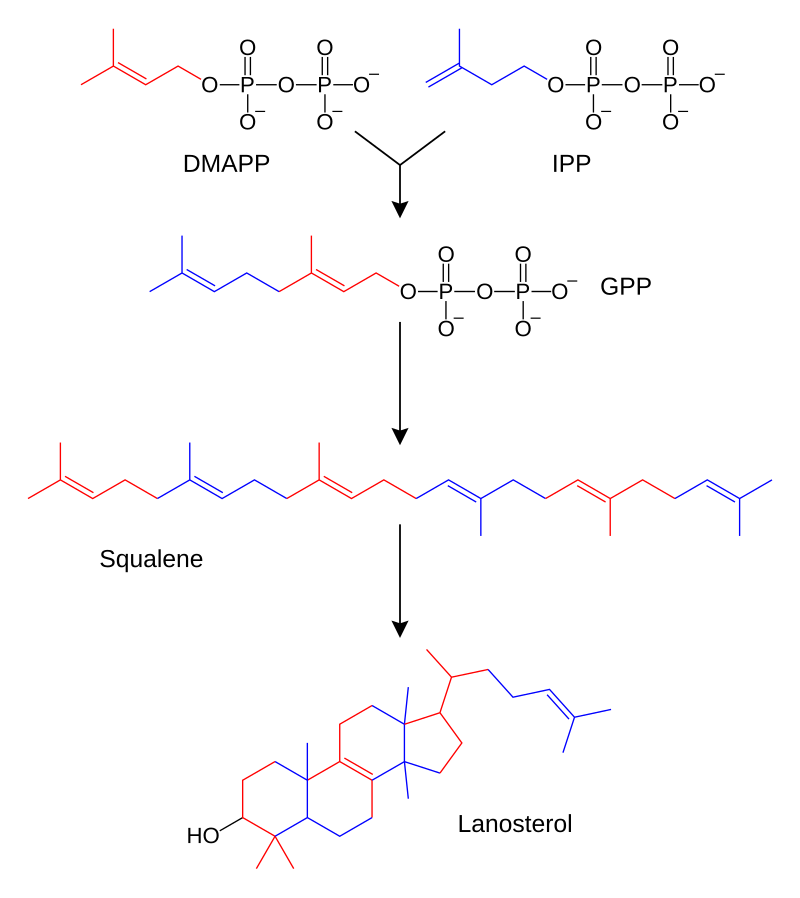
نسخة مبسطة من مسار تصنيع ستيرويد. أثزيلت بعض المركبات الوسيطة من أجل الوضوح.
يصنع
الأحماضَ الدهنية إنزيمُ مصنع الحمض الدهني الذي يبلمر ثم يختزل وحدات
أسيتيل مرافق الإنزيم-أ. حلقات الأسيل الموجودة في الأحماض الدهنية تتمدد
بحلقة من التفاعلات التي تضيف مجموعة الأسيل، وتختزلها إلى كحول، ثم تنزع
منها الماء لتحولها إلى مجموعة ألكين ثم تختزلها مجددا إلى مجموعة ألكان.
تنقسم إنزيمات التصنيع الحيوي للأحماض الدهنية إلى مجموعتين: في الحيوانات
والفطريات، تُنفّذ كل تفاعلات تصنيع الحمض الدهني ببروتين واحد متعدد
الوظائف، أما في بلاستيدات النبات وفي البكتيريا يؤدي إنزيم مختلف كل خطوة
في المسار.تربين، وتربينويد هما فئة كبيرة من الدهون التي تشمل كاروتينات
وتشكل الفئة الأكبر من المنتجات الطبيعية للنبات. تُصنع تلك المركبات
بتجميع وتعديل وحدات إيزوبرين التي تتبرع بها مركبات طليعية متفاعلة. تفاعل
مهم يستخدم المركبات المتبرعة بإيزوبرين هو تصنيع الستيرويد. حيث تنضم
وحدات إيزوبرين لبعضها لبعض لتكوين سكوالين ثم تُطوى لتشكيل مجموعة من
الحلقات لتكون لانوستيرول. يمكن بعد ذلك تحويل لانوستيرول ‘لى ستيرويدات
أخرى مثل كولسترول وإرغوستيرول.
البروتيناتتختلف الكائنات في قدرتها على
تصنيع الـ20 حمض أميني المشتركة. تستطيع أغلب البكتيريا والنباتات تصنيع
العشرين حمض جميعهم، إلا أن الثدييات تستطيع تصنيع 11 حمض أميني غير ضروري،
لذلك فإن 9 أحماض أمينية ضرورية يجب الحصول عليها من الغذاء. بعض
الطفيليات البسيطة، مثل بكتيريا المفطورة الرئوية، تفتقد القدرة على تصنيع
أي من الأحماض الأمينية وتحصل على أحماضها الأمينية مباشرة من العائل.
تُصنع كل الأحماض الأمينية من مركبات وسطية في تحلل الجلوكوز، ودورة حمض
الستريك، أو مسار فوسفات البنتوز. يتيج النيتروجينَ حمضُ الجلوتاميك
والجلوتامين. يعتمد تصنيع الأحماض الأمينية على تكوين حمض كيتو ألفا
المناسب، الذي تُنقل مجموعة الأمين له لتكوين حمض أميني.تُصنع البروتينات
من الأحماض الأمينية عن طريق ضم بعضها لبعض في سلسلة من الروابط الببتيدية.
يملك كل بروتين مختلف تسلسل فريد من الأحماض الأمينية: وهذا هو تركيبه
الأولي. تماما كما يمكن دمج حروف الأبجدية لتكوين عدد لا نهائي من الكلمات،
يمكن ربط الأحماض الأمينية في تسلسلات مختلفة لتكوين عدد هائل من
البروتينات. يُصنّع البروتينات من الأحماض الأمينية التي نشطها الارتباط
بجزئ حمض نووي ريبوزي ناقل برابطة إستر. يُنتج هذا المركب الطليعي في تفاعل
يعتمد على أدينوسين ثلاثي الفوسفات. يعد هذا المركب ركيزة للريبوسوم، الذي
ينضم إلى الحمض الأميني على سلسلة البروتين المطوي ، باستخدام معلومات
التسلسل في الحمض النووي الريبوزي الرسول.
تصنيع وإنقاذ
النوكليوتيدتتكون النوكليوتيدات من أحماض أمينية، وثنائي أكسيد الكربون،
وحمض الفورميك في مسارات تتطلب كميات كبيرة من الطاقة الأيضية. بناء على
ذلك، تمتلك أغلب الكائنات أنظمة فعالة لإنقاذ النوكليوتيدات المتكونة.
يُصنّع البيورين كنيوكليوسيد (قواعد مرتبطة بالريبوز). كل من الأدينين،
والغوانين يُصنع من مركب نيوكلوسيد طليعي إينوسين أحادي الفوسفات، الذي
يُصنع باستخدام ذرات من الأحماض الأمينية جلايسين، وجلوتامين، وحمض
الأسبارتيك. في المقابل، يُصنّع بيريميدين من أوروتيت، الذي يُصنع من
جلوتامين وحمض الأسبارتيك.
الدخيل الحيوي وأيض الأكسدة والاختزالتتعرض
كل الكائنات الحية باستمرار إلى مركبات لا يمكنهم استخدامها كغذاء وتكون
ضارة إذا تراكمت في الخلايا، حيث لا توجد وظيفة أيضية له. تلك المركبات
التي يحتمل أن تكون ضارة تسمى الغريب الحيوي أو الدخيل الحيوي. الدخائل
الحيوي مثل الأدوية المصنعة، والسموم الطبيعية، والمضادات الحيوية تُزال
سميتها بمجموعة من الإنزيمات الأيضية للغريب الحيوي. في الإنسان، تشمل تلك
الإنزيمات مؤكسدات سيتوكروم بي450، وغلوكويورنوسايل ترانسفيراز، وجلوتاثيون
أس-ترانسفيراز. يعمل هذا الجهاز من الإنزيمات في 3 مراحل لأكسدة الغريب
الحيوي أولاً (المرحلة 1) ثم ربط مجموعات قابلة للذوبان في الماء للجزئ
(المرحلة 2). الغريب الحيوي المعدل القابل للذوبان في الماء يمكن بعد ذلك
ضخة خارج الخلايا وفي الكائنات متعددة الخلايا يمكن أيضه أكثر من ذلك قبل
إخراجه (المرحلة 3). في علم البيئة، تلك التفاعلات مهمة بالأخص في التحلل
الحيوي الميكروبي للملوثات والمعالجة الحيوية للأرض الملوثة وتسرب النفط.
العديد من تلك التفاعلات الميكروبية تتواجد في كائنات متعددة الخلايا، ولكن
بسبب التنوع الكبير في أنواع الميكروبات فإن تلك الكائنات قدرة على
التعامل مع نطاق أوسع بكثير من الدخائل الحيوية مقارنة بالكائنات متعددة
الخلايا، ويمكنها حتى تحليل الملوثات العضوية الثابتة مثل مركبات الكلوريد
العضوي.مشكلة متعلقةبالكائنات الهوائية هي الإجهاد التأكسدي. هنا، العمليات
التي تشملفسفرة تأكسدية وتكوين روابط ثنائية الكبريتيد خلال تطوي البروتين
تنتج أنواع الأكسجين التفاعلية مثل بيروكسيد الهيدروجين. تلك المؤكسدات
الضارة تُزيلُها مستقلبات مضادة للتأكسد مثل جلوتاثيون وإنزيمات مثل
كاتالاز وبيروكسيداز.
الديناميكا الحرارية للكائنات الحيةيجب أن تخضع
الكائنات الحية لقوانين الديناميكا الحرارية، التي تصف انتقال الحرارة
والشغل. ينص قانون الديناميكا الحراري الثاني على أنه في أي نظام مغلق، لا
يمكن أن تقل كمية الإنتروبيا. رغم أن التعقيد المدهش للكائنات الحية يبدو
أنه يتعارض مع هذا القانون، فإن الحياة ممكنة لأن جميع الكائنات تعد نظام
مفتوح يتبادل المادة والطاقة مع الأشياء المحيطة به. بالتالي فإن الأنظمة
الحية ليست في حالة توازن ترموديناميكي، وإنما هي أنظمة مبددة تحافظ على
حالة التعقيد الكبير بالتسبب في زيادة أكبر في الإنتروبيا في بيئاتها. يحقق
أيض الخلية ذلك من خلال الربط بين العمليات التلقائية للتقويض والعمليات
غير التلقائية للابتناء. بمصطلحات الديناميكا الحرارية، يحافظ الأيض على
النظام عن طريق خلق الفوضى.
التنظيم والتحكم
نظرًا لأن بيئة أغلب
الكائنات تتغير باستمرار، يجب أن تُنظم تفاعلات الأيض تنظيمًا دقيقًا
للحفاظ على مجموعة ثابتة من الظروف داخل الخلايا، فيما يعرف باسم
الاستتباب. يسمح تنظيم الأيض كذلك للكائنات الحية بالاستجابة للإشارات
والتفاعل تفاعلًا نشطًا مع بيئاتهم. مبدآن مترابطان ارتباطًا كبيرًا مهمان
للغاية في فهم كيفية التحكم في المسارات الأيضية. الأول، أن تنظيم إنزيم ما
في مسار ما هو كيف أن نشاطه يزيد ويقل استجابة لإشارات. الثاني، أن التحكم
الذي يبذله ذلك الإنزيم هو تأثير تلك التغيرات في نشاطه على المعدل الكلي
للمسار. على سبيل المثال، قد يُظهر إنزيم ما تغيرات كبيرة في نشاطه (أي أنه
منظم تنظيمًا كبيرًا) لكن إذا كانت تلك التغيرات لها أثر بسيط على معدل
المسار الأيضي، فإن هذا الإنزيم ليس مساهما في التحكم في ذلك المسار.
💥

تأثير
الانسولين على استيعاب وأيض الجلوكوز. يرتبط الإنسولين بالمستقبل الخاص به
(1)، والذي بدوره يبدأ العديد من تتاليات تنشيط البروتين (2). يشمل ذلك:
نقل ناقل الجلوكوز 4 إلى الغشاء الخلوي ودخول الجلوكوز (3)، وتصنيع
الغلايكوجين (4)، وتحلل الجلوكوز (5) وتصنيع الأحماض الدهنية (6).
توجد
العديد من مستويات تنظيم الأيض. في التنظيم الداخلي، يقوم المسار الأيضي
بتنظيم نفسه ليستجيب للتغيرات في مستويات الركائز أو المنتجات، على سبيل
المثال، نقص كمية المادة المنتجة يزيد التدفق عبر المسار من أجل التعويض.
يتضمن هذا النوع من التنظيم عادة تنظيم تفارغي لنشاطات العديد من الإنزيمات
في المسار. يتضمن التحكم الخارجي في كائن متعدد الخلايا أن تقوم خلية
بتعيير أيضها استجابة لإشارات من خلايا أخرى. تلك الإشارات عادة تكون في
صورة رسل ذائبة مثل الهرمونات وعوامل النمو وتكتشفها مستقبلات على سطح
الخلية. تُبثّ بعد ذلك تلك الإشارات داخل الخلية بأنظمة الرسول الثاني التي
تشارك غالبا في فسفرة البروتينات.نموذج مفهوم جدا للتحكم الخارجي هو تنظيم
أيض الجلوكوز بهرمون الإنسولين. يُنتج الإنسولين استجابة لارتفاع سكر
الدم. ارتباط الهرمون بمستقبلة الإنسولين على الخلايا ينشط سلسة من
البروتين كيناز التي تؤدي لاستيعاب الخلايا للجلوكوز من الدم وتحويله إلى
جزيئات تخزين مثل الأحماض الدهنية والغلايكوجين. يتحكم نشاط إنزيم
فوسفوريلاز في أيض الغلايكوجين، وهو الإنزيم الذي يكسر الغلايكوجين،
وغلايكوجين سينثاز، الإنزيم الذي يصنعه. تُنظم تلك الإنزيمات تنظيمًا
متبادلًا، حيث تثبط الفسفرة غلايكوجين سينثاز، وتنشط فوسفوريلاز. يتسبب
الإنسولين في تصنيع الغلايكوجين بتنشيط فوسفاتاز البروتين والتسبب في نقص
فسفرة تلك الإنزيمات.
التطور
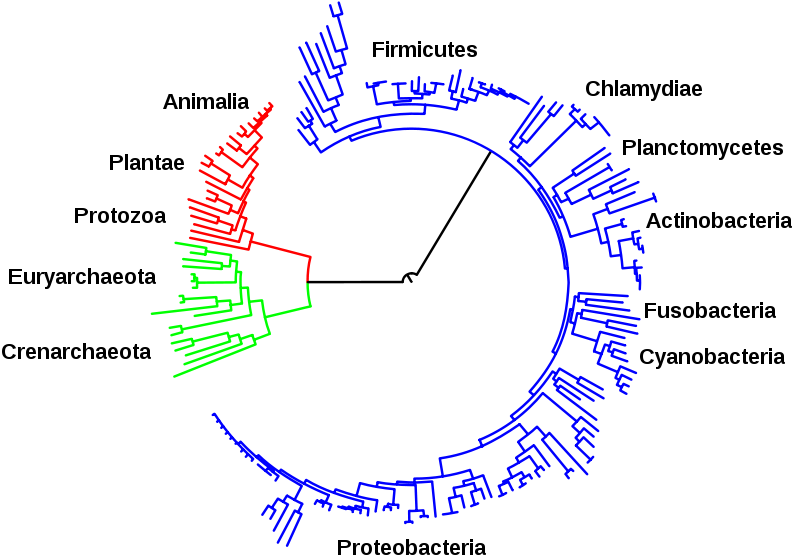 شجرة
تطور تظهر الأصل المشترك للكائنات الحية من النطاقات الثلاثة. البكتيريا
ملونة بالأزرق، وحقيقيات النوى بالأحمر، والبكتيريا القديمة بالأخضر.
المواقف النسبية لبعض الشعب المدرجة تظهر حول الشجرة.
شجرة
تطور تظهر الأصل المشترك للكائنات الحية من النطاقات الثلاثة. البكتيريا
ملونة بالأزرق، وحقيقيات النوى بالأحمر، والبكتيريا القديمة بالأخضر.
المواقف النسبية لبعض الشعب المدرجة تظهر حول الشجرة.
المسارات
المركزية للأيض المذكورة سابقًا، مثل تحلل الجلوكوز، ودورة حمض الستريك،
تتواجد في النطاقات الثلاثة للكائنات الحية وكانت متواجدة كذلك في السلف
الشامل الأخير. كانت خلية السلف الشامل بدائية النوى ومولدة للميثان غالبا
وبها الكثير من أيض الحمض الأميني، والنوكوليوتيد، والسكريات، والدهون. قد
يكون الإبقاء على هذه المسارات القديمة خلال التطور المتأخر ناتجا عن أن
هذه التفاعلات كانت الحل الأمثل لمشاكلهم الأيضية الخاصة، مع مسارات مثل
تحلل الجلوكوز ودورة حمض الستريك تنتج نواتجها النهائية بفعالية عالية
وبعدد محدود من الخطوات. قد تكون المسارات الأولى في الأيض القائم على
الإنزيمات جزءًا من أيض نوكليوتيد البيورين، فيما كانت مسارات الأيض
السابقة جزءًا منفرضية عالم الحمض النووي الريبوزي القديمة.اقتُرحت العديد
من النماذج لوصف آليات تطور مسارات الأيض الحديثة. تشمل تلك النماذج إضافات
متتابعة لإنزيمات جديدة لمسارات قديمة قصيرة، وتضاعف ثم تشعب المسارات
بالكامل بالإضافة لتوظيف الانزيمات الموجودة مسبقا وتجميعها في مسار تفاعل
جديد. الأهمية النسبية لتلك الآليات غير واضحة، إلا أن دراسات جينومية
أظهرت أن الإنزيمات في مسار ما من المحتمل أن يكون لها سلف مشترك، ما يقترح
أن العديد من المسارات قد تطورت خطوة بخطوة مع تكوُّن وظائف جديدة من
الخطوات الموجودة سابقًا في المسار. نموذج بديل ظهر من دراسات تتبع تطور
تركيب البروتيان في شبكة الأيض، اقترح ذلك النموذج أن الإنزيمات تُوظّف
توظيفًا واسعًا، واستعارة إنزيمات لتأدية وظائف مشابهة في مسارات أيضية
مختلفة. تؤدي عملية التوظيف تلك إلى تنوع في التطور الإنزيمي. احتمال ثالث
هو أن بعض أجزاء الأيض قد تتواجد في «وحدات» يمكن إعادة استخدماها في
مسارات مختلفة وتؤدي نفس الوظائف على جزيئات مختلفة.بالإضافة لتطور مسارات
أيضية جديدة، يمكن أن يسبب التطور كذلك فقد بعض الوظائف الأيضية. على سبيل
المثال، في بعض الديدان فُقدت العمليات الأيضية غير الضرورية للحياة،
وعوضًا عنها يمكن استغلال الأحماض الأمينية، والنوكليوتيدات، والسكريات
الموجودة مسبقًا في العائل. يمكن ملاحظة أمثلة مشابهة لفقد القدرات الأيضية
في كائنات المعايشة الجوانية.
الاستقصاء والمعالجة

شبكة أيض لدورة حمض الستريك فيرشاد أذن الفأر. تظهر الإنزيمات والمستقلبات في صورة مربعات حمراء والتفاعلات بينهما كخطوط سوداء.
يُدرس
الأيض تقليديًا بمقاربة اختزالية تركز على مسار أيضي واحد. استعمال
القائفات المشعة مفيد خصوصًا في تعقب الكائن بالكامل، وعلى مستوى النسيج،
والخلية، والذي يحدد المسار من المركب الطليعي حتى الناتج النهائي عن طريق
التعرف على الوسائط والمنتجات المعلمة بمادة مشعة. الإنزيمات التي تحفز تلك
التفاعلات الكيميائية يمكن بعد ذلك تنقيتها ودراسة حركياتها واستجابتها
للمثبطات. مقاربة موازية هي التعرف على الجزئيات الصغيرة في خلية أو نسيج،
المجموعة الكاملة من تلك الجزيئات تسمى ميتابولوم. عمومًا تعطي تلك
الدراسات نظرة جيدة على تركيب ووظيفة المسارات الأيضية البسيطة، لكنها غير
كافية عند تطبيقها على أنظمة أكثر تعقيدا مثل أيض خلية كاملة.يمكن الحصول
على فكرة عن مدى تعقيد شبكات الأيض في الخلايا التي تحتوي على آلاف
الإنزيمات المختلفة عن طريق الشكل الموضح في الصورة الذي يعرض التفاعلات
بين 43 بروتينًا و40 مستقلبًا فقط: توفر تسلسلات الجينومات قوائم تحتوي على
ما يصل إلى 45,000 جين. مع ذلك، من الممكن الآن استخدام تلك البيانات
الجينومية لإعادة تشكيل شبكات كاملة من التفاعلات الكيميائية الحيوية
وإنتاج نماذج رياضية أكثر كلية قد تشرح وتتوقع سلوكياتهم. تلك النماذج قوية
بشكل خاص حين تستخدم لدمج بيانات المسار والمستقلب المحصول عليها عبر
الطرق التقليدية مثل التعبير الجيني من الدراسات البروتيومية ومصفوفة دي إن
إيه الدقيقة. باستخدام تلك الطرق، أُنتج نموذج لأيض الإنسان، ما سيساعد في
اكتشاف أدوية مستقبلية وأبحاث الكيمياء الحيوية. تستخدم تلك النماذج الآن
في تحليل الشبكات، لتصنيف أمراض الإنسان في مجموعات تتشارك في بروتينات أو
مستقلبات مشتركة.تعد شبكات الأيض البكتيرية مثالا صارخًا على تنظيم ربطة
العنق على شكل قوس،
وهو تركيب قادر على إدخال نطاق واسع من المغذيات
وإنتاج مجموعة كبيرة من المنتجات والجزيئات الكبيرة المعقدة باستخدام
تداولات وسيطة مشتركة قليلة نسبيًا.
تطبيق تكنولوجي كبير لتلك
المعلومات هو الهندسة الأيضية. وفيها تُعدّل بعض الكائنات كالخميرة، أو
النباتات، أو البكتيريا جينيًا لجعلهم أكثر فائدة في التكنولوجيا الحيوية
وللمساعدة في إنتاج أدوية مثل المضادات الحيوية أو الكيماويات الصناعية مثل
حمض الشيكيميك. تهدف تلك التعديلات الجينية عادة لتقليل كم الطاقة
المستخدم لإنتاج المنتج، وزيادة الإنتاجية، وتقليل مخلفات الإنتاج.
التاريخ 
الأيض لأرسطو كنموذج تدفق مفتوح
يحتوي
كتاب أجزاء الحيوان لأرسطو على تفاصيل كافية عن وجهة نظره بشأن الأيض تكفي
لصنع نموذج تدفق مفتوح. حيث آمن أن كل مرحلة من العملية، تُحول فيها مواد
من الطعام، مع إطلاق حرارة باعتباره العنصر التقليدي للحريق، وفضلات تُخرَج
في صورة بول، أو براز، أو صفراء.وصف ابن النفيس الأيض في عام 1260 في
روايته الرسالة الكاملية في السيرة النبوية والتي احتوت عبارة «كل من الجسم
وأجزاءه في حالة مستمرة من الانحلال والبناء، لذلك هي حتما تمر بتغيير
دائم.» يمتد تاريخ الدراسة العلمية للتمثيل الغذائي لعدة قرون وانتقل من
دراسة الحيوانات بالكامل في الدراسات المبكرة، لدراسة التفاعلات الأيضية
المفردة في الكيمياء الحيوية الحديثة. نشر التجاربَ المخططة الأولى لأيض
الإنسان في 1614 سانتوريو سانتوري في كتابه حرق الطب الساكن.
وصف
فيه كيف وزن نفسه قبل وبعد الأكل، والنوم، والعمل، وممارسة الجنس، والصوم،
والشرب، والإخراج. حيث وجد أن أغلب الطعام الذي تناوله قد فقد عبر ما أسماه
«عرق غير
ملموس». 💥

سانتوريو سانتوري في ميزانه القباني، من كتاب حرق الطب الساكن، نشر أول مرة في 1614
في
تلك الدراسات المبكرة، لم يحدث التعرف على آليات تلك العمليات الأيضية
وكان من المعتقد أن هناك قوة حيوية تنشط الأنسجة الحية. في القرن الـ19،
عند دراسة تخمير السكر إلى كحول بواسطة الخميرة، استنتج لويس باستور أن
التخمير حفزته موادٌ في خلايا الخميرة أسماها «مخمرات». كتب أن «التخمير
الكحولي هو عمل مرتبط بحياة وتنظيم خلايا الخميرة، وليس مع موت أو تعفن
الخلايا.» هذا الاكتشاف، إلى جانب ما نشره فريدرش فولر في 1828 عن بحث حول
التصنيع الكيميائي لليوريا،
وكونها أول مركب عضوي يحضر بالكامل من
مركبات طليعية غير عضوية أثبتا أن المركبات العضوية والتفاعلات الكيميائية
الموجودة في الخلية لا تختلف من حيث المبدأ عن أي جزء من الكيمياء.
اكتشف
الإنزيمات في بدايات القرن الـ20 إدوارد بوخنر فهو ما فصل دراسة تفاعلات
الأيض الكيميائية عن الدراسة البيولوجية للخلايا، وأشار ببدء الكيمياء
الحيوية. نما حجم المعرفة الكيميائية الحيوية بسرعة خلال أوائل القرن
الـ20. أحد أكثر علماء الكيمياء الحيوية الجدد المثمرين وقتها كان هانس
كريبس الذي قدم إسهامات هائلة في دراسة الأيض. اكتشف كريبس دورة اليوريا
ولاحقًا، بالتعاون مع هانز كورنبيرج، دورة حمض الستريك ودورة الجلايكسولات.
تمت
مساعدة أبحاث الكيمياء الحيوية الحديثة بشكل كبير بسبب تطور التقنيات
الحديثة مثل الاستشراب، ودراسة البلورات بالأشعة السينية، ومطيافية الرنين
المغناطيسي النووي، والوسم النظيري، والمجهر الإلكتروني. سمحت تلك التقنيات
باكتشاف والتحليل المفصل للعديد من الجزيئات والمسارات الأيضية في
الخلايا.
انظر أيضًابروتين دهني منخفض الكثافة
بروتين دهني مرتفع الكثافة
كوليسترول
أيض مفرط
بيروفات سينثاز
أيض الحمض العصاري
أيض فيضي
أيض جرياني
معدل الأيض الأساسي
متلازمة إعادة التغذية
خطأ أيضي خلقي
سلسلة تنفس
تاريخ علم الكيمياء الحيوية
نظرية الجذور الحرة والتشيخ
مرونة الأيض
سينثيز بيتا-كيتوأسيل- ACP .

ليست هناك تعليقات:
إرسال تعليق